| Академия » Статьи » Билеты/вопросы/ответы » Педиатрия |
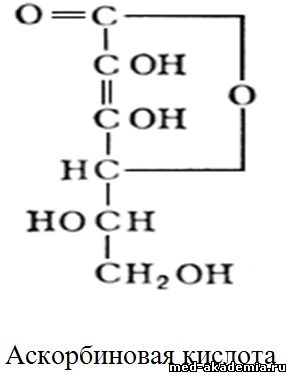
АСКОРБИНОВАЯ КИСЛОТА
|
В 1933 г. двумя учеными Хирстом Эйлером независимо друг от друга была найдена структурная формула аскорбиновой кислоты, оказавшаяся отличной от структуры молекулы глюкоруновой кислоты:
Первые исследователи химических свойств витамина С отметили его способность легко окисляться в водных растворах растворенным кислородом воздуха. Обстоятельное изучение редуцирующего фактора растительных соков, оказавшегося аскорбиновой кислотой, провел Тильманс. Он установил, например, что редуцирующий фактор может существовать в двух формах: восстановленной и обратимо-окисленной. При мягком окислении восстановленной формы она переходит в обратимо-окисленную, которая действием восстановителей вновь может превращаться в первоначальную, восстановленную форму. При хранении сока, в котором редуцирующий фактор находился в обратимо-окисленной форме, его способность переходить в восстановленную форму со временем утрачивается. Действие сильных окислителей, таких, как молекулярный кислород, приводит к необратимому окислению редуцирующего фактора, после чего уже никакие восстановители не могут дать процессу обратный ход, чтобы перевести конечный продукт реакции в первоначальную форму. Тильманс в свое время отметил, что необратимое окисление редуцирующего фактора сопровождается полной утратой растительным соком антицинготных свойств, в то время как при обратимом окислении редуцирующего фактора свойство сока предупреждать и излечивать цингу сохраняется. Это позволило Тильмансу приписать редуцирующие и антицинготные свойства одному и тому же веществу, витамину С. Когда витамин С был, наконец, выделен и установлена его химическая природа, явления, описанные Тильмансом, нашли свое объяснение как свойства аскорбиновой кислоты, вытекающие из структуры ее молекулы. Оказалось, что способность витамина С к обратимому окислению зависит от наличия в составе его молекулы диэнольной группировки. Первоначальный продукт окисления аскорбиновой кислоты – дегидроаскорбиновая кислота, которая и является обратимо-окисленной формой аскорбиновой кислоты, обладает всеми свойствами витамина С. Химические же свойства этих двух веществ различны. В то время как аскорбиновая кислота имеет сильные кислотные свойства, дегидроаскорбиновая кислота утрачивает их вместе с двумя энольными атомами водорода. Отсутствие двойной связи между атомами углерода делает молекулу дегидроаскорбиновой кислоты довольно неустойчивой к гидролизу, особенно в щелочной и даже слабокислой среде. При гидролизе вначале разрывается лактонное кольцо и образуется 2,3-дикето-1-гулоновая кислота, которая затем окисляется с разрывом углеродного скелета молекулы и образованием 1-треоновой и щавелевой кислот. Ни 2,3-дикето-1-гулоновая кислота, ни продукты ее разложения не обладают свойствами витамина С. Изучение процесса окисления аскорбиновой кислоты показало, что в водных растворах в присутствии кислорода воздуха этот процесс не идет без катализаторов – ионов меди и серебра. Однако в обычной водопроводной воде ионы этих металлов всегда присутствуют, во всяком случае, ионы меди, в достаточном для каталитического действия количестве. |
| Вы можете прокомментировать статью | |